亲爱的读者们,你是否曾经对那些神奇的化学实验感到好奇?今天,我要带你走进一个充满奥秘的世界——制取二氧化碳的实验。没错,就是那个我们日常生活中无处不在的气体!接下来,就让我们一起通过一段特别详细的实验视频,揭开这个气体的神秘面纱吧!
实验前的准备
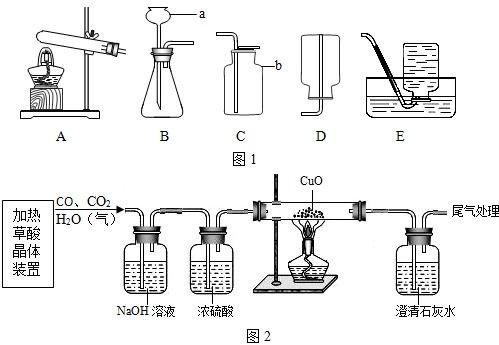
在进行实验之前,我们需要准备以下材料:
1. 稀盐酸(浓度约为6mol/L)
2. 石灰石(碳酸钙)
3. 试管
4. 烧杯
5. 橡皮塞
6. 导管
7. 水槽
8. 集气瓶
准备好这些材料后,我们就可以开始这场奇妙的实验之旅了。
实验步骤
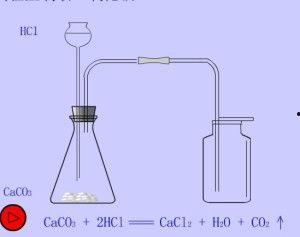
1. 装填石灰石:将适量的石灰石放入试管中,注意不要装得太满,以免影响实验效果。
2. 加入稀盐酸:用滴管将稀盐酸缓慢滴入装有石灰石的试管中。你会看到石灰石表面开始产生气泡,这是因为碳酸钙与盐酸反应生成了二氧化碳气体。
3. 连接导管:将导管的一端插入试管中,另一端连接到集气瓶。确保连接牢固,以免实验过程中气体泄漏。
4. 收集二氧化碳:将集气瓶放入水槽中,观察气体收集情况。当集气瓶内充满二氧化碳气体时,用橡皮塞封住瓶口。
5. 验证二氧化碳:将一根点燃的木条伸入集气瓶中,你会看到火焰迅速熄灭。这是因为二氧化碳不支持燃烧,具有灭火作用。
6. 实验结束:将实验器材清洗干净,妥善存放。
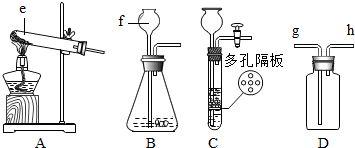
实验原理
这个实验的原理其实很简单。石灰石(碳酸钙)与稀盐酸反应,生成二氧化碳气体、水和氯化钙。化学方程式如下:
CaCO3 2HCl → CO2↑ H2O CaCl2
在这个反应中,二氧化碳气体以气泡的形式从石灰石表面逸出,通过导管进入集气瓶中。
实验视频解析
为了让大家更直观地了解这个实验,我找到了一段非常详细的实验视频。视频中,实验者详细介绍了实验步骤、注意事项以及实验现象。以下是对视频内容的简要解析:
1. 实验步骤:视频中的实验者按照上述步骤进行实验,操作熟练,讲解清晰。
2. 实验现象:实验过程中,石灰石表面产生大量气泡,二氧化碳气体被成功收集到集气瓶中。当点燃的木条伸入集气瓶时,火焰迅速熄灭,验证了二氧化碳的灭火作用。
3. 注意事项:实验者提醒观众注意安全,如佩戴防护眼镜、手套等。同时,实验过程中要避免气体泄漏,以免造成安全隐患。
4. 实验拓展:视频还介绍了二氧化碳的其他应用,如灭火、制冷等。
通过这段实验视频,我们不仅了解了制取二氧化碳的实验过程,还学习了二氧化碳的物理和化学性质。这个实验简单易行,适合广大化学爱好者进行实践。希望这篇文章和视频能给你带来启发,让你在化学的世界里畅游!